Osteoporosi post-menopausa
L’osteoporosi (OP) menopausale causata dalla carenza estrogenica, implica un aumentato riassorbimento osseo, con conseguente diminuzione della densità minerale (BMD) e della resistenza ossea, che si traducono in aumentato rischio di fratture da fragilità. Queste provocano dolore, perdita di funzionalità, diminuzione della qualità e dell’aspettativa di vita e sono una causa maggiore di morbilità e mortalità.
Approccio Diagnostico
Anamnesi accurata per valutare la presenza di fattori di rischio:
- età avanzata (> 65 anni);
- basso peso (BMI < 18.5 kg/m2);
- pregresse fratture: in presenza di fratture da fragilità di rachide, femore, avambraccio, omero e bacino, si pone diagnosi di OP anche con valori di T-score alla densitometria ossea (DEXA) > -2.5 DS;
- familiarità;
- utilizzo di glucocorticoidi (> 5 mg/die di prednisone o equivalenti per 3 mesi);
- utilizzo di altri farmaci che influiscono negativamente sulla massa ossea (inibitori dell’aromatasi, ormoni tiroidei a dosi soppressive, chemioterapia, ciclosporina, eparina non frazionata e a basso peso molecolare, antidepressivi, tiazolidinedioni, alcuni anti-convulsivanti, inibitori di pompa protonica, ecc);
- abitudine a fumo e alcool;
- artrite reumatoide;
- alterazioni del ciclo mestruale (ipogonadismo, menopausa precoce);
- frequenti cadute;
- cause di OP secondaria: pregresso trapianto d’organo, iperparatiroidismo primario, insufficienza renale cronica (IRC), diabete, anoressia nervosa, ipopituitarismo, malassorbimento, pregressa chirurgia bariatrica,
immobilizzazione, ipertiroidismo non trattato, pneumopatie croniche, HIV, sindrome di Cushing, osteogenesi imperfetta, sindrome di Marfan, malattia di Gaucher, ecc.
Esame obiettivo alla ricerca di eventuali deformazioni rachidee o dolorabilità alla palpazione delle apofisi spinose.
Indagini strumentali
- DEXA: ogni riduzione del T-score al di sotto dello 0 implica un rischio duplicato o triplicato di sviluppare fratture da fragilità. L’OP viene diagnosticata per valori di T-score alla DEXA < -2.5, mentre valori compresi tra -1 e -2.49 sono riferibili a osteopenia. L’esame densitometrico deve essere proposto se ci troviamo di fronte a donne in post-menopausa con età: o ≥ 65 anni; o < 65 anni se si associano uno o più fattori di rischio (tra quelli precedentemente elencati). Nella paziente con frattura da fragilità non è necessario eseguire la DEXA per fare diagnosi di OP, anche se ottenere dei valori basali risulta utile per monitorare l’efficacia della terapia nel follow-up.
- Rx morfometrica della colonna vertebrale: deve essere eseguita se c’è un forte sospetto per fratture vertebrali, sulla base della storia clinica o dell’esame obiettivo (es riduzione di altezza > 3.8 cm) o se la presenza di una o più fratture potrebbe modificare la scelta di trattamento.
Valutazione del rischio fratturativo
Per impostare correttamente una terapia anti-osteoporotica, può essere utile eseguire, oltre alle indagini sopra citate, una stima del rischio fratturativo attraverso appositi strumenti di calcolo.
L’indice FRAX (fracture risk assessment tool) stima la probabilità a 10 anni di sviluppare una frattura osteoporotica maggiore (MOF) o una frattura di femore sulla base della presenza dei fattori di rischio, e può essere o meno integrato dai valori densitometrici per avere una stima più precisa. Vengono considerate ad “alto rischio” pazienti con rischio di MOF ≥ 20% o di frattura di femore ≥ 3%. Il trabecular bone score (TBS) consiste in una misurazione indiretta e qualitativa, a partire dall’immagine DEXA, della micro-architettura dell’osso vertebrale tramite l’utilizzo di appositi software. Il TBS predice il rischio fratturativo indipendentemente dai valori di BMD, tuttavia non può essere utilizzato da solo per porre diagnosi, ma risulta utile se valutato in aggiunta a FRAX e DEXA, specialmente nelle pazienti con BMD normale. Non vi è tuttavia consenso sui cut-off per il TBS.
Esami ematochimici
L’utilizzo varia in base alla situazione clinica della paziente e serve a escludere eventuali cause di osteoporosi secondaria e controindicazioni ai trattamenti farmacologici. Prima di iniziare la terapia è consigliato di valutare almeno i livelli sierici di creatinina, calcio, fosfato, albumina, 25-OH D3, PTH, fosfatasi alcalina, glicemia, emocromo ed elettroforesi proteica. I marcatori di rimodellamento osseo si suddividono in marcatori di formazione (propeptide Nterminale del collagene di tipo I – PINP –, osteocalcina, fosfatasi alcalina, propeptide C-terminale del collagene di tipo I) e di riassorbimento (telopeptide C del collagene di tipo I – CTX-I –, telopeptide N del collagene di tipo I – NTX-I). Pur non essendo raccomandato routinariamente, il loro dosaggio risulta utile nel monitoraggio del trattamento dopo 3 o 6 mesi dall’inizio della somministrazione del farmaco, per stabilire risposta e aderenza della paziente alla terapia (10), mentre non è indicato il dosaggio in fase diagnostica. Quando si indaga il metabolismo osseo andrebbero dosati almeno un marcatore di riassorbimento e uno di formazione ossea: la IOF raccomanda l’utilizzo di CTX-I e PINP, ma la scelta può variare a seconda della disponibilità locale e dei costi.
Trattamento
Tutti i farmaci utilizzati nella terapia dell’osteoporosi riducono il rischio di fratture vertebrali e alcuni agiscono anche diminuendo il rischio di fratture non vertebrali e di fratture di femore. Partendo dallo stile di vita, molte LG raccomandano per le donne con osteoporosi post-menopausale un apporto di calcio compreso tra i 1000 e 1200 mg/die, preferibilmente ottenuto dalla dieta, e di vitamina D tra 400 e 1000 UI/die. La terapia farmacologica deve essere scelta sulla base di diversi fattori, quali gravità dell’osteoporosi e rischio fratturativo, ma anche in base a fattori e preferenze specifici della paziente.
I farmaci a disposizione si suddividono in:
- anti-riassorbitivi: riducono il riassorbimento osseo interagendo con gli osteoclasti, inibendone la proliferazione, la funzionalità e favorendone l’apoptosi;
- anabolici: aumentano la neoformazione ossea. Sono indicati nelle donne considerate a rischio “molto alto”, cioè con T-score < -3, o con fratture vertebrali multiple, o in presenza di una frattura da fragilità già verificatasi con T-score -2.5;
- a duplice azione (anti-riassorbitiva + anabolica): anticorpi monoclonali che inibiscono la sclerostina.
La tabella riassume gli effetti collaterali e le controindicazioni dei trattamenti farmacologici attualmente utilizzati nella terapia dell’osteoporosi.
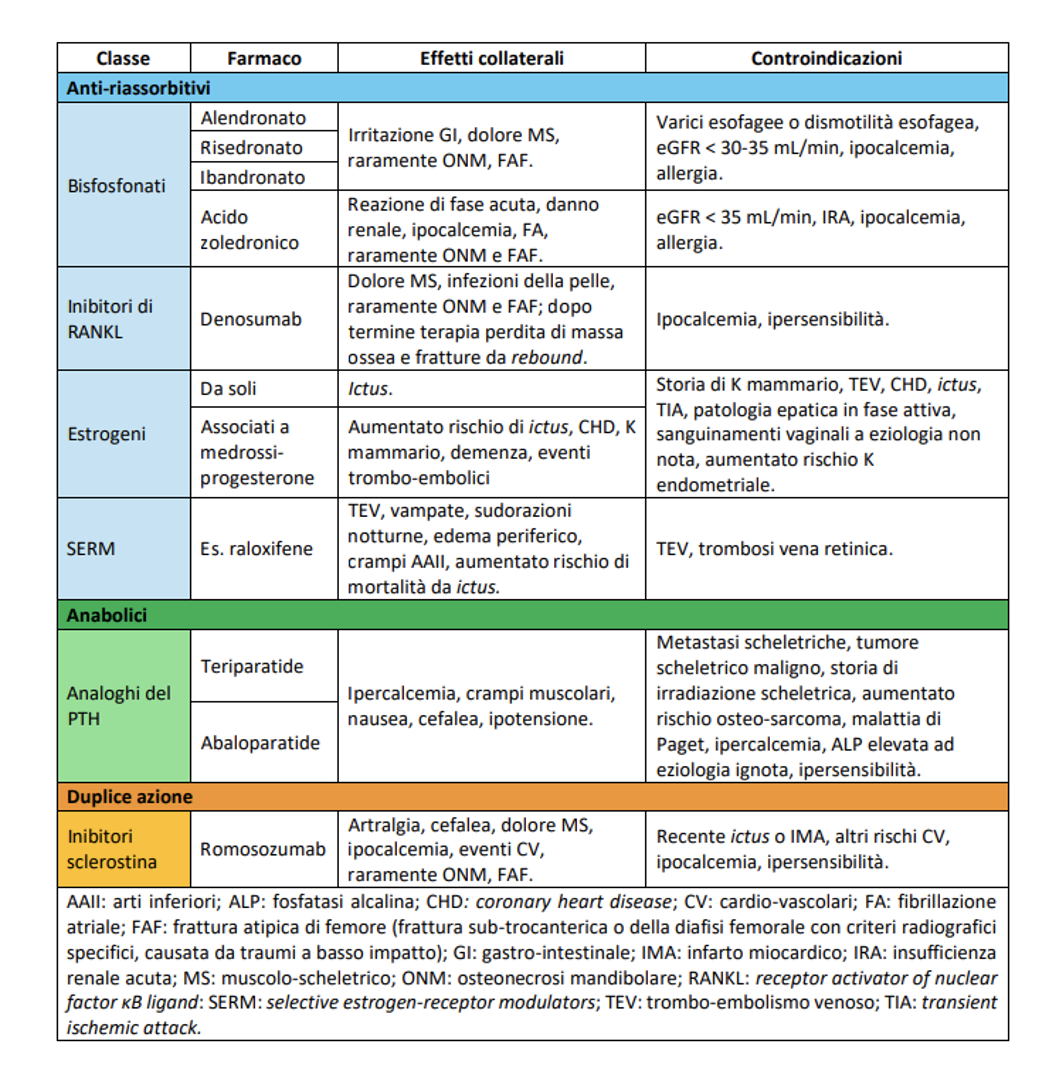
Bisfosfonati
Tutti i bisfosfonati riducono il rischio di fratture vertebrali, di femore e non vertebrali, ad esclusione dell’ibandronato che agisce prevalentemente sulla colonna. L’acido zoledronico, inoltre, quando viene somministrato entro 90 giorni da un evento fratturativo e per una durata di 3 anni, riduce anche il rischio di mortalità correlato all’evento.
Per quanto riguarda la durata del trattamento, tutte le LG sono concordi nel dare indicazione a proseguire il trattamento con bisfosfonati orali per almeno 5 anni, dopo i quali si può prendere in considerazione l’interruzione della terapia in base alla rivalutazione del rischio fratturativo:
- se rimane alto o molto alto, è indicata la prosecuzione della terapia per altri 5 anni;
- se è da basso a moderato, si può sospendere il trattamento per un periodo più o meno lungo. Tale scelta sembra particolarmente vantaggiosa per la riduzione del rischio di FAF ( frattura atipica femore: l’incidenza decresce all’aumentare del tempo trascorso dall’ultima dose ricevuta).
Le LG consigliano di eseguire una rivalutazione del rischio ogni 2-4 anni durante il periodo di “vacanza terapeutica”, ricominciando il trattamento in caso di declino della BMD clinicamente significativo, frattura, o se dovessero presentarsi altre condizioni che vanno ad aumentare il rischio fratturativo.
Nel caso di pazienti ad alto rischio, inoltre, le LG consigliano di considerare la pausa terapeutica solo dopo 6-10 anni di stabilità della BMD.
Nelle pazienti che fanno uso di acido zoledronico ev ogni 12 mesi, la rivalutazione del rischio deve essere eseguita dopo 3 anni dall’inizio della terapia: in caso di alto rischio, si può proseguire con la somministrazione per altri 3 anni, oppure considerare un nuovo farmaco.
Denosumab
Secondo le LG, il suo utilizzo è indicato in donne con OP post-menopausale a rischio alto e molto alto di sviluppare fratture da fragilità. Risulta efficace nell’aumentare la BMD e nel ridurre il rischio di frattura.
L’uso di denosumab è associato all’insorgenza di ipocalcemia in pazienti con IRC o carenza di vitamina D; risulta pertanto importante il monitoraggio di quest’ultima, oltre che della funzionalità renale e del calcio, nei pazienti in trattamento con tale farmaco.
Non è stata stabilita una durata massima di terapia con denosumab, ma l’Endocrine Society raccomanda la rivalutazione del rischio fratturativo dopo 5 o 10 anni di terapia, in base alla quale decidere se continuare con lo stesso farmaco o cambiarlo in favore di un’altra molecola.
Vi è inoltre preoccupazione riguardo l’accelerato riassorbimento osseo e la rapida perdita di massa ossea che si verificano in seguito all’interruzione del trattamento o alla somministrazione ritardata di questo farmaco (con un ritardo > 16 settimane rispetto alla somministrazione prevista con cadenza semestrale), motivo per cui a volte non viene considerato come prima scelta in pazienti che hanno altre opzioni terapeutiche. Le LG specificano che in seguito all’interruzione della terapia con denosumab, deve essere avviata quella di mantenimento con bisfosfonati, per ridurre l’aumentato rischio di sviluppare fratture vertebrali multiple. Tra l’ultima dose di denosumab e la prima di bisfosfonati, siano essi orali o endovenosi, non devono passare più di 6 mesi.
Analoghi del PTH
Le LG ne limitano l’uso a pazienti:
- con rischio molto alto di sviluppare fratture da fragilità;
- con effetti collaterali non accettabili provocati da altri trattamenti;
- non responsivi ad altre terapie.
Alcuni studi ne hanno dimostrato la maggior efficacia rispetto ai bisfosfonati nell’aumentare la BMD e nel diminuire l’incidenza di fratture vertebrali.
La durata della terapia con analoghi del PTH non deve eccedere i due anni, a meno che non vi sia alla rivalutazione un rischio di frattura stabilmente alto o molto alto, o in pazienti non responsivi ad altri trattamenti (ma questa estensione in Italia non è consentita).
Al termine del trattamento con teriparatide (PTH 1-34) o abaloparatide (PTHrP 1-34) è indicata una terapia antiriassorbitiva, altrimenti la BMD acquistata durante il trattamento viene persa nel giro di circa un anno.
Romosozumab
Recentemente approvato per il trattamento dell’OP post-menopausale, si è dimostrato maggiormente efficace rispetto a tutte le altre terapie, sia nell’azione anti-riassorbitiva che anabolizzante. Il suo utilizzo è limitato alle pazienti con rischio molto alto, per un massimo di 12 mesi. Anche in questo caso, per poter mantenere i benefici al termine della terapia con romosozumab deve essere utilizzato un farmaco anti-riassorbitivo.
Associazioni e terapia sequenziale
La combinazione nell’utilizzo di denosumab e teriparatide si è dimostrata più efficace rispetto ai farmaci utilizzati singolarmente nell’aumentare la BMD a livello di femore e colonna; tuttavia, attualmente, questa associazione non è prevista dalle LG.
Vi sono dati limitati riguardo l’utilizzo in sequenza di trattamenti farmacologici differenti. Anche se gli antiriassorbitivi sono considerati da utilizzare in prima linea, attenuano o ritardano il guadagno di massa ossea che si verifica in risposta all’utilizzo di farmaci anabolizzanti. In seguito al trattamento con bisfosfonati, comunque, per favorire l’incremento della BMD si è dimostrato maggiormente efficace passare a romosozumab piuttosto che a teriparatide. Deve essere evitato il passaggio da denosumab a teriparatide, a causa della perdita di massa ossea.
FOCUS: L’OSTEONECROSI DELLA MANDIBOLA (ONM)
L’ONM da farmaci è caratterizzata da un’area di esposizione dell’osso mandibolare, che non guarisce dopo 8 settimane dall’identificazione da parte di un operatore sanitario, in pazienti che hanno fatto uso continuo di bisfosfonati o di un altro agente anti-riassorbitivo, senza essere stati mai precedentemente esposti a radiazioni della regione della testa e del collo . È molto rara con i dosaggi di bisfosfonati utilizzati nella terapia dell’osteoporosi. La natura di questa condizione, potenzialmente debilitante, è riconducibile a un’infezione cronica, generalmente causata da batteri appartenenti alla flora microbica orale, che porta alla necrosi e all’esposizione del tessuto osseo, con scarsa tendenza alla risoluzione. Spesso i pazienti che vengono a conoscenza di questo effetto collaterale dei farmaci anti-riassorbitivi sono restii iniziare il trattamento, influenzando quindi il medico nella scelta terapeutica.
Cosa può fare il medico?
- evitare o ritardare questa terapia in pazienti con problemi odontoiatrici attivi al momento della prescrizione;
- prima di iniziare la terapia, eseguire una valutazione del rapporto rischio/beneficio nei pazienti con fattori di rischio (richiedere il nulla-osta odontoiatrico);
- raccomandare igiene orale e controlli odontoiatrici periodici;
- qualora la paziente sviluppi ONM, è opportuno considerare, ove possibile, l’interruzione temporanea del trattamento fino a completa risoluzione della condizione e fino a quando i fattori di rischio non siano attenuati.
Conclusioni
La gestione dell’OP post-menopausale richiede l’approfondita conoscenza della paziente per una presa in carico appropriata e personalizzata. Oltre ad arrivare alla corretta diagnosi nel minor tempo possibile, l’obiettivo fondamentale del medico deve essere la prevenzione delle fratture da fragilità, tramite un approccio treat-totarget per diminuire efficacemente il rischio fratturativo.
Le LG prese in esame sono concordi sul fatto che la diagnosi si basi sulla presenza di fratture da fragilità o BMD < -2.5, individuate tramite l’utilizzo rispettivamente di morfometria vertebrale e DEXA.
Le raccomandazioni al trattamento invece differiscono lievemente: se tutte le LG considerano appropriato trattare donne in menopausa con un T-score < -2.5, non vi è unanimità nella gestione delle pazienti osteopeniche (T-score fra -1 e -2.4) con aumentato rischio di sviluppare fratture da fragilità.
RICHIEDI UN APPUNTAMENTO
Compila il modulo per richiedere una vita con il Dr. Casini
Chiama ora e Prenota una Visita
Appuntamento Telefonico
WhatsApp Roma
Indirizzo
Via Tiraboschi, 20 – 00141 – Roma
WhatsApp Ciampino
Indirizzo
Via della Repubblica, 3 – 00043 – Ciampino
